ခေတ်သစ်ဆေးပညာနယ်ပယ်တွင် ပဋိဇီဝဆေးများသည် အထင်ရှားဆုံးတိုးတက်မှုများထဲမှတစ်ခုဖြစ်ကြောင်း သက်သေပြခဲ့ပြီး အဏုဇီဝပိုးဝင်ခြင်းနှင့်ဆက်စပ်သော ဖြစ်ပွားမှုနှုန်းနှင့် သေဆုံးမှုနှုန်းကို သိသိသာသာလျှော့ချပေးခဲ့သည်။ ဘက်တီးရီးယားပိုးဝင်ခြင်း၏ ဆေးခန်းရလဒ်များကို ပြောင်းလဲနိုင်စွမ်းရှိသော ၎င်းတို့၏စွမ်းရည်သည် မရေမတွက်နိုင်သော လူနာများ၏ သက်တမ်းကို တိုးစေခဲ့သည်။ ခွဲစိတ်မှုများ၊ ခန္ဓာကိုယ်အတွင်း ထည့်သွင်းခြင်း၊ အစားထိုးခြင်းနှင့် ဓာတုကုထုံးအပါအဝင် ရှုပ်ထွေးသော ဆေးဘက်ဆိုင်ရာလုပ်ထုံးလုပ်နည်းများတွင် ပဋိဇီဝဆေးများသည် အရေးပါပါသည်။ သို့သော် ပဋိဇီဝဆေးယဉ်ပါးသော ရောဂါပိုးများ ပေါ်ပေါက်လာခြင်းသည် တိုးပွားလာနေသော စိုးရိမ်မှုတစ်ခုဖြစ်ပြီး အချိန်ကြာလာသည်နှင့်အမျှ ဤဆေးဝါးများ၏ ထိရောက်မှုကို လျော့ကျစေသည်။ အဏုဇီဝမျိုးကွဲများ ဖြစ်ပေါ်လာသည်နှင့်အမျှ ပဋိဇီဝဆေးယဉ်ပါးမှုဖြစ်ရပ်များကို ပဋိဇီဝဆေးအမျိုးအစားအားလုံးတွင် မှတ်တမ်းတင်ထားသည်။ အဏုဇီဝပိုးသတ်ဆေးများမှ ထုတ်ပေးသော ရွေးချယ်မှုဖိအားသည် ခံနိုင်ရည်ရှိသော မျိုးကွဲများ မြင့်တက်လာစေရန် ပံ့ပိုးပေးခဲ့ပြီး ကမ္ဘာ့ကျန်းမာရေးအတွက် သိသာထင်ရှားသော စိန်ခေါ်မှုတစ်ရပ် ဖြစ်စေသည်။
ပဋိဇီဝဆေးယဉ်ပါးမှုပြဿနာကို တိုက်ဖျက်ရန်အတွက် ပဋိဇီဝဆေးအသုံးပြုမှုကို လျှော့ချခြင်းနှင့်အတူ ခံနိုင်ရည်ရှိသော ရောဂါပိုးများပျံ့နှံ့မှုကို ထိန်းချုပ်သည့် ထိရောက်သော ကူးစက်ရောဂါထိန်းချုပ်ရေးမူဝါဒများကို အကောင်အထည်ဖော်ရန် အရေးကြီးပါသည်။ ထို့အပြင် အခြားကုသမှုနည်းလမ်းများအတွက်လည်း အရေးတကြီးလိုအပ်ပါသည်။ Hyperbaric Oxygen Therapy (HBOT) သည် ဤအခြေအနေတွင် အလားအလာကောင်းသော နည်းလမ်းတစ်ခုအဖြစ် ပေါ်ထွက်လာခဲ့ပြီး သတ်မှတ်ထားသော ဖိအားအဆင့်တွင် ၁၀၀% အောက်ဆီဂျင်ကို အချိန်ကာလတစ်ခုအတွင်း ရှူရှိုက်ခြင်းပါဝင်ပါသည်။ ရောဂါပိုးများအတွက် အဓိကကုသမှု သို့မဟုတ် ဖြည့်စွက်ကုသမှုအဖြစ် HBOT သည် ပဋိဇီဝဆေးယဉ်ပါးသော ရောဂါပိုးများကြောင့် ဖြစ်ပေါ်လာသော ပြင်းထန်သောရောဂါပိုးများကို ကုသရာတွင် မျှော်လင့်ချက်အသစ်များ ပေးစွမ်းနိုင်ပါသည်။
ဤကုထုံးကို ရောင်ရမ်းခြင်း၊ ကာဗွန်မိုနောက်ဆိုဒ်အဆိပ်သင့်ခြင်း၊ နာတာရှည်ဒဏ်ရာများ၊ သွေးလည်ပတ်မှုနည်းသောရောဂါများနှင့် ရောဂါပိုးများအပါအဝင် အခြေအနေအမျိုးမျိုးအတွက် အဓိက သို့မဟုတ် အခြားရွေးချယ်စရာကုသမှုအဖြစ် ပိုမိုအသုံးပြုလာကြသည်။ ရောဂါပိုးများကုသရာတွင် HBOT ၏ လက်တွေ့အသုံးချမှုများသည် အလွန်နက်ရှိုင်းပြီး လူနာများအတွက် အဖိုးမဖြတ်နိုင်သော အကျိုးကျေးဇူးများကို ပေးစွမ်းသည်။

ရောဂါပိုးဝင်ခြင်းတွင် Hyperbaric Oxygen Therapy ၏ လက်တွေ့အသုံးချမှုများ
လက်ရှိအထောက်အထားများအရ HBOT ကို သီးခြားကုသမှုနှင့် နောက်ဆက်တွဲကုသမှုနှစ်မျိုးလုံးအဖြစ် အသုံးပြုခြင်းကို ခိုင်မာစွာထောက်ခံထားပြီး ရောဂါကူးစက်ခံရသူများအတွက် သိသာထင်ရှားသော အကျိုးကျေးဇူးများကို ပေးစွမ်းသည်။ HBOT ကာလအတွင်း သွေးလွှတ်ကြောအောက်ဆီဂျင်ဖိအားသည် 2000 mmHg အထိ မြင့်တက်လာနိုင်ပြီး ရလဒ်အနေဖြင့် အောက်ဆီဂျင်-တစ်ရှူးဖိအားမြင့်မားခြင်းသည် တစ်ရှူးအောက်ဆီဂျင်အဆင့်ကို 500 mmHg အထိ မြင့်တက်စေနိုင်သည်။ ထိုကဲ့သို့သော အကျိုးသက်ရောက်မှုများသည် ischemic ပတ်ဝန်းကျင်တွင် တွေ့ရှိရသော ရောင်ရမ်းမှုတုံ့ပြန်မှုများနှင့် microcirculatory disruptions များကို ပျောက်ကင်းစေရန်အပြင် compartment syndrome ကို စီမံခန့်ခွဲရာတွင် အထူးတန်ဖိုးရှိပါသည်။
HBOT သည် ကိုယ်ခံအားစနစ်အပေါ် မှီခိုနေရသော အခြေအနေများကိုလည်း သက်ရောက်မှုရှိနိုင်သည်။ သုတေသနပြုချက်များအရ HBOT သည် ကိုယ်ခံအားရောဂါလက္ခဏာများနှင့် အင်တီဂျင်ကြောင့်ဖြစ်ပေါ်သော ကိုယ်ခံအားတုံ့ပြန်မှုများကို နှိမ်နင်းနိုင်ပြီး ကိုယ်ခံအားတုံ့ပြန်မှုများကို ပြုပြင်ပြောင်းလဲနေစဉ်တွင် လင့်ဖိုဆိုက်များနှင့် သွေးဖြူဥများ၏ သွေးလည်ပတ်မှုကို လျှော့ချခြင်းဖြင့် ဆဲလ်အစားထိုးမှုခံနိုင်ရည်ကို ထိန်းသိမ်းရန် ကူညီပေးသည်။ ထို့အပြင်၊ HBOTကုသခြင်းကို အထောက်အကူပြုသည်နာတာရှည်အရေပြားအနာများတွင် ပြန်လည်ကောင်းမွန်လာစေရန်အတွက် အရေးကြီးသောလုပ်ငန်းစဉ်တစ်ခုဖြစ်သည့် angiogenesis ကိုလှုံ့ဆော်ပေးခြင်းဖြင့်ဖြစ်သည်။ ဤကုထုံးသည် ဒဏ်ရာပျောက်ကင်းခြင်းတွင် မရှိမဖြစ်လိုအပ်သောအဆင့်ဖြစ်သည့် collagen matrix ဖွဲ့စည်းမှုကိုလည်း အားပေးသည်။
အချို့သော ရောဂါပိုးများ၊ အထူးသဖြင့် necrotizing fasciitis၊ osteomyelitis၊ နာတာရှည် soft tissue infections နှင့် infectious endocarditis ကဲ့သို့သော နက်ရှိုင်းပြီး ကုသရန်ခက်ခဲသော ရောဂါပိုးများကို အထူးဂရုပြုရမည်။ HBOT ၏ အသုံးအများဆုံး လက်တွေ့အသုံးချမှုများထဲမှ တစ်ခုမှာ anaerobic သို့မဟုတ် resistant bacteria များကြောင့် မကြာခဏဖြစ်ပွားလေ့ရှိသော အရေပြား-soft tissue infections နှင့် osteomyelitis အတွက် ဖြစ်သည်။
၁။ ဆီးချိုခြေထောက်ပိုးဝင်ခြင်း
ဆီးချိုခြေထောက်ဆီးချိုရောဂါရှိသူများတွင် အနာများသည် အဖြစ်များသော နောက်ဆက်တွဲပြဿနာတစ်ခုဖြစ်ပြီး လူဦးရေ၏ ၂၅% အထိ သက်ရောက်မှုရှိသည်။ ဤအနာများတွင် ရောဂါပိုးများ မကြာခဏဖြစ်ပွားလေ့ရှိပြီး (ဖြစ်ပွားမှု၏ ၄၀% မှ ၈၀% အထိရှိသည်) ရောဂါဖြစ်ပွားမှုနှင့် သေဆုံးမှုနှုန်း မြင့်တက်လာစေသည်။ ဆီးချိုခြေထောက်ပိုးဝင်ခြင်း (DFIs) တွင် အောက်ဆီဂျင်မဲ့ဘက်တီးရီးယားပိုးများ အမျိုးမျိုးကို ဖော်ထုတ်တွေ့ရှိထားသည့် polymicrobial ပိုးများ ပါဝင်လေ့ရှိသည်။ ဖိုင်ဘရိုဘလတ်စ်လုပ်ဆောင်ချက်ချို့ယွင်းချက်များ၊ ကော်လာဂျင်ဖွဲ့စည်းမှုပြဿနာများ၊ ဆဲလ်ခုခံအားယန္တရားများနှင့် ဖာဂိုဆိုက်လုပ်ဆောင်ချက်အပါအဝင် အချက်အမျိုးမျိုးသည် ဆီးချိုရောဂါရှိသူများတွင် အနာကျက်ခြင်းကို အနှောင့်အယှက်ဖြစ်စေနိုင်သည်။ လေ့လာမှုများစွာက အရေပြားအောက်ဆီဂျင်ချို့တဲ့ခြင်းသည် DFIs နှင့်ဆက်စပ်သော ခြေလက်ဖြတ်တောက်ခြင်းအတွက် ပြင်းထန်သောအန္တရာယ်အချက်တစ်ခုအဖြစ် ဖော်ထုတ်ခဲ့သည်။
DFI ကုသမှုအတွက် လက်ရှိရွေးချယ်စရာများထဲမှ တစ်ခုအဖြစ်HBOT သည် ဆီးချိုခြေထောက်အနာများအတွက် ပျောက်ကင်းမှုနှုန်းကို သိသိသာသာ မြှင့်တင်ပေးသည်ဟု သတင်းများထွက်ပေါ်ခဲ့ပြီး နောက်ပိုင်းတွင် ခြေလက်ဖြတ်တောက်ခြင်းနှင့် ရှုပ်ထွေးသော ခွဲစိတ်ကုသမှုများ လိုအပ်ချက်ကို လျှော့ချပေးပါသည်။ ၎င်းသည် ခြေထောက်ခွဲစိတ်မှုနှင့် အရေပြားအစားထိုးခြင်းကဲ့သို့သော အရင်းအမြစ်များစွာ အသုံးပြုရသည့် လုပ်ထုံးလုပ်နည်းများအတွက် လိုအပ်ချက်ကို လျှော့ချပေးရုံသာမက ခွဲစိတ်မှုနည်းလမ်းများနှင့် နှိုင်းယှဉ်ပါက ကုန်ကျစရိတ်နည်းပါးပြီး ဘေးထွက်ဆိုးကျိုး အနည်းဆုံးဖြစ်သည်။ Chen နှင့် အဖွဲ့၏ လေ့လာမှုတစ်ခုအရ HBOT ၁၀ ကြိမ်ထက်ပို၍ ကုသမှုခံယူခြင်းသည် ဆီးချိုဝေဒနာရှင်များတွင် အနာကျက်နှုန်း ၇၈.၃% တိုးတက်ကောင်းမွန်လာစေကြောင်း ပြသခဲ့သည်။
၂။ ပျော့ပျောင်းသောတစ်ရှူးပိုးဝင်ခြင်း
တစ်ရှူးပျက်စီးခြင်း (NSTIs) များသည် များသောအားဖြင့် aerobic နှင့် anaerobic ဘက်တီးရီးယားပိုးများ ပေါင်းစပ်မှုကြောင့် ဖြစ်ပေါ်လာသော polymicrobial များဖြစ်ပြီး ဓာတ်ငွေ့ထုတ်လုပ်မှုနှင့် မကြာခဏ ဆက်စပ်နေပါသည်။ NSTIs များသည် အတော်လေး ရှားပါးသော်လည်း ၎င်းတို့၏ လျင်မြန်စွာ တိုးတက်လာမှုကြောင့် သေဆုံးမှုနှုန်း မြင့်မားပါသည်။ အချိန်မီနှင့် သင့်လျော်သော ရောဂါရှာဖွေခြင်းနှင့် ကုသမှုသည် အပြုသဘောဆောင်သော ရလဒ်များ ရရှိရန် အဓိကသော့ချက်ဖြစ်ပြီး HBOT ကို NSTIs များကို စီမံခန့်ခွဲရန်အတွက် နောက်ဆက်တွဲနည်းလမ်းတစ်ခုအဖြစ် အကြံပြုထားသည်။ အလားအလာရှိသော ထိန်းချုပ်ထားသော လေ့လာမှုများ မရှိခြင်းကြောင့် NSTIs များတွင် HBOT အသုံးပြုခြင်းနှင့်ပတ်သက်၍ အငြင်းပွားမှုများ ရှိနေဆဲဖြစ်သော်လည်း၊၎င်းသည် NSTI လူနာများတွင် ရှင်သန်နှုန်းနှင့် ကိုယ်တွင်းအင်္ဂါများ ထိန်းသိမ်းမှု တိုးတက်ကောင်းမွန်လာခြင်းနှင့် ဆက်စပ်နေနိုင်ကြောင်း အထောက်အထားများက အကြံပြုထားသည်။နောက်ကြောင်းပြန်လေ့လာမှုတစ်ခုအရ HBOT ခံယူနေသော NSTI ဝေဒနာရှင်များတွင် သေဆုံးမှုနှုန်း သိသိသာသာ လျော့ကျသွားကြောင်း ညွှန်ပြနေသည်။
၁.၃ ခွဲစိတ်မှုနေရာတွင် ရောဂါပိုးဝင်ခြင်း
SSI များကို ရောဂါပိုးဝင်သည့်နေရာပေါ် မူတည်၍ အမျိုးအစားခွဲခြားနိုင်ပြီး aerobic နှင့် anaerobic bacteria နှစ်မျိုးလုံးအပါအဝင် ရောဂါပိုးအမျိုးမျိုးမှ ပေါ်ပေါက်လာနိုင်သည်။ ပိုးသတ်နည်းစနစ်များ၊ ကြိုတင်ကာကွယ်သည့် ပဋိဇီဝဆေးများအသုံးပြုခြင်းနှင့် ခွဲစိတ်ကုသမှုလုပ်ငန်းများတွင် တိုးတက်မှုများရှိသော်လည်း SSI များသည် ဆက်လက်ဖြစ်ပွားနေသော နောက်ဆက်တွဲပြဿနာတစ်ခုအဖြစ် ရှိနေဆဲဖြစ်သည်။
အာရုံကြောနှင့်ကြွက်သား ကျောရိုးစောင်းခြင်းခွဲစိတ်မှုတွင် နက်ရှိုင်းသော SSI များကိုကာကွယ်ရာတွင် HBOT ၏ထိရောက်မှုကို သိသာထင်ရှားသောပြန်လည်သုံးသပ်ချက်တစ်ခုတွင် စုံစမ်းစစ်ဆေးခဲ့သည်။ ခွဲစိတ်မှုမတိုင်မီ HBOT သည် SSI ဖြစ်ပွားမှုနှုန်းကို သိသိသာသာလျှော့ချပေးနိုင်ပြီး အနာကျက်ခြင်းကို အထောက်အကူပြုနိုင်သည်။ ဤကျူးကျော်မဟုတ်သောကုထုံးသည် အနာတစ်ရှူးများတွင် အောက်ဆီဂျင်အဆင့်မြင့်မားလာသည့်ပတ်ဝန်းကျင်ကို ဖန်တီးပေးပြီး ၎င်းသည် ရောဂါပိုးများကို တိုက်ဖျက်သည့် အောက်ဆီဒေးရှင်းသတ်ဖြတ်ခြင်းလုပ်ဆောင်ချက်နှင့် ဆက်စပ်နေသည်။ ထို့အပြင် ၎င်းသည် SSI များဖွံ့ဖြိုးတိုးတက်မှုကို အထောက်အကူပြုသည့် သွေးနှင့် အောက်ဆီဂျင်အဆင့်နိမ့်ကျမှုကို ကိုင်တွယ်ဖြေရှင်းပေးသည်။ အခြားကူးစက်မှုထိန်းချုပ်ရေးဗျူဟာများအပြင် HBOT ကို အူမကြီးခွဲစိတ်မှုများကဲ့သို့သော သန့်ရှင်းသောညစ်ညမ်းမှုရှိသော ခွဲစိတ်မှုများအတွက် အထူးသဖြင့် အကြံပြုထားသည်။
၁.၄ မီးလောင်ဒဏ်ရာများ
အပူလောင်ဒဏ်ရာများသည် အပူလွန်ကဲခြင်း၊ လျှပ်စစ်စီးကြောင်း၊ ဓာတုပစ္စည်းများ သို့မဟုတ် ရောင်ခြည်တို့ကြောင့် ဖြစ်ပေါ်လာသော ဒဏ်ရာများဖြစ်ပြီး ရောဂါဖြစ်ပွားမှုနှင့် သေဆုံးမှုနှုန်း မြင့်မားစေနိုင်သည်။ HBOT သည် ပျက်စီးနေသော တစ်ရှူးများတွင် အောက်ဆီဂျင်ပမာဏကို မြှင့်တင်ပေးခြင်းဖြင့် အပူလောင်ဒဏ်ရာများကို ကုသရာတွင် အကျိုးရှိပါသည်။ တိရစ္ဆာန်နှင့် ဆေးခန်းလေ့လာမှုများတွင် ရောထွေးနေသော ရလဒ်များကို တင်ပြထားသော်လည်းမီးလောင်ဒဏ်ရာကုသမှုတွင် HBOT ၏ထိရောက်မှုမီးလောင်ဒဏ်ရာရသူ ၁၂၅ ဦးပါဝင်သည့် လေ့လာမှုတစ်ခုအရ HBOT သည် သေဆုံးမှုနှုန်း သို့မဟုတ် ပြုလုပ်ခဲ့သော ခွဲစိတ်မှုအရေအတွက်အပေါ် သိသာထင်ရှားသော အကျိုးသက်ရောက်မှုမရှိကြောင်း ပြသခဲ့သော်လည်း ပျမ်းမျှပျောက်ကင်းချိန် (၄၃.၈ ရက်နှင့် နှိုင်းယှဉ်ပါက ၁၉.၇ ရက်) ကို လျှော့ချပေးခဲ့ကြောင်း ဖော်ပြသည်။ HBOT ကို ပြည့်စုံသော မီးလောင်ဒဏ်ရာစီမံခန့်ခွဲမှုနှင့် ပေါင်းစပ်ခြင်းဖြင့် မီးလောင်ဒဏ်ရာရသူများတွင် sepsis ကို ထိရောက်စွာ ထိန်းချုပ်နိုင်ပြီး ပျောက်ကင်းချိန်ကို တိုတောင်းစေပြီး အရည်လိုအပ်ချက်ကို လျှော့ချပေးပါသည်။ သို့သော် ကျယ်ပြန့်သော မီးလောင်ဒဏ်ရာများကို စီမံခန့်ခွဲရာတွင် HBOT ၏ အခန်းကဏ္ဍကို အတည်ပြုရန် နောက်ထပ် ကျယ်ပြန့်သော အနာဂတ်သုတေသန လိုအပ်ပါသည်။
၁.၅ အရိုးအဆစ်ရောင်ရောဂါ
အရိုးအဆစ်ရောင်ရောဂါသည် ဘက်တီးရီးယားပိုးမွှားများကြောင့် မကြာခဏဖြစ်ပွားလေ့ရှိသော အရိုး သို့မဟုတ် အရိုးတွင်းခြင်ဆီပိုးဝင်ခြင်းတစ်ခုဖြစ်သည်။ အရိုးများသို့ သွေးထောက်ပံ့မှု နည်းပါးခြင်းနှင့် ခြင်ဆီထဲသို့ ပဋိဇီဝဆေးများ ဝင်ရောက်မှု အကန့်အသတ်ရှိခြင်းတို့ကြောင့် အရိုးအဆစ်ရောင်ရောဂါကို ကုသခြင်းသည် ခက်ခဲနိုင်ပါသည်။ နာတာရှည် အရိုးအဆစ်ရောင်ရောဂါသည် နာတာရှည်ရောဂါပိုးများ၊ အနည်းငယ်ရောင်ရမ်းခြင်းနှင့် အရိုးတစ်ရှူးများ ပျက်စီးခြင်းတို့ဖြင့် သွင်ပြင်လက္ခဏာရှိသည်။ သင့်လျော်သော ကုသမှုခံယူနေသော်လည်း ဆက်လက်ဖြစ်ပွားသော သို့မဟုတ် ထပ်ခါတလဲလဲဖြစ်ပွားသော နာတာရှည်အရိုးပိုးဝင်ခြင်းကို ရည်ညွှန်းသည်။
HBOT သည် ကူးစက်ခံရသော အရိုးတစ်ရှူးများတွင် အောက်ဆီဂျင်ပမာဏကို သိသိသာသာ တိုးတက်ကောင်းမွန်စေကြောင်း ပြသထားသည်။ များစွာသော case series နှင့် cohort လေ့လာမှုများက HBOT သည် osteomyelitis လူနာများအတွက် လက်တွေ့ရလဒ်များကို မြှင့်တင်ပေးကြောင်း ဖော်ပြသည်။ ၎င်းသည် ဇီဝဖြစ်စဉ်ဆိုင်ရာ လုပ်ဆောင်ချက်ကို မြှင့်တင်ခြင်း၊ ဘက်တီးရီးယားပိုးမွှားများကို နှိမ်နင်းခြင်း၊ ပဋိဇီဝဆေးအာနိသင်ကို မြှင့်တင်ခြင်း၊ ရောင်ရမ်းမှုကို လျှော့ချခြင်းနှင့် အနာကျက်ခြင်းကို မြှင့်တင်ခြင်း အပါအဝင် ယန္တရားအမျိုးမျိုးမှတစ်ဆင့် လုပ်ဆောင်ပုံရသည်။လုပ်ငန်းစဉ်များ။ HBOT ပြီးနောက်၊ နာတာရှည်၊ ပြန်လည်ကောင်းမွန်ရန်ခက်ခဲသော အရိုးရောင်ရောဂါရှိသူ ၆၀% မှ ၈၅% သည် ရောဂါပိုးကူးစက်မှုကို နှိမ်နင်းနိုင်သည့် လက္ခဏာများ ပြသကြသည်။
၁.၆ မှိုပိုးဝင်ခြင်း
ကမ္ဘာတစ်ဝှမ်းတွင် လူဦးရေ သုံးသန်းကျော်သည် နာတာရှည် သို့မဟုတ် ကျူးကျော်ဝင်ရောက်လာသော မှိုပိုးဝင်ခြင်းများကို ခံစားနေရပြီး နှစ်စဉ် သေဆုံးသူ ၆၀၀,၀၀၀ ကျော်ရှိသည်။ မှိုပိုးဝင်ခြင်းအတွက် ကုသမှုရလဒ်များသည် ပြောင်းလဲနေသော ကိုယ်ခံအားအခြေအနေ၊ အခြေခံရောဂါများနှင့် ရောဂါပိုးများ၏ အဆိပ်အတောက်ဖြစ်စေသော ဝိသေသလက္ခဏာများကဲ့သို့သော အချက်များကြောင့် မကြာခဏ ထိခိုက်လေ့ရှိသည်။ HBOT သည် ၎င်း၏ ဘေးကင်းမှုနှင့် ကျူးကျော်ဝင်ရောက်ခြင်းမရှိသော သဘောသဘာဝကြောင့် ပြင်းထန်သော မှိုပိုးဝင်ခြင်းများတွင် ဆွဲဆောင်မှုရှိသော ကုထုံးရွေးချယ်မှုတစ်ခု ဖြစ်လာနေသည်။ လေ့လာမှုများအရ HBOT သည် Aspergillus နှင့် Mycobacterium tuberculosis ကဲ့သို့သော မှိုပိုးများကို ထိရောက်စွာ တိုက်ဖျက်နိုင်ကြောင်း ဖော်ပြသည်။
HBOT သည် Aspergillus ၏ biofilm ဖွဲ့စည်းမှုကို ဟန့်တားခြင်းဖြင့် မှိုပိုးများကို တိုက်ဖျက်သည့် အာနိသင်ကို မြှင့်တင်ပေးပြီး superoxide dismutase (SOD) မျိုးဗီဇများ ချို့တဲ့သော မျိုးကွဲများတွင် ထိရောက်မှု မြင့်တက်လာသည်ကို သတိပြုမိပါသည်။ မှိုပိုးကူးစက်မှုများအတွင်း အောက်ဆီဂျင်နည်းပါးသော အခြေအနေများသည် မှိုပိုးများ ပို့ဆောင်ရာတွင် စိန်ခေါ်မှုများ ဖြစ်စေပြီး HBOT မှ အောက်ဆီဂျင်ပမာဏ မြင့်တက်လာခြင်းသည် အလားအလာရှိသော အကျိုးရှိသော ကြားဝင်ဆောင်ရွက်မှုတစ်ခု ဖြစ်စေသော်လည်း နောက်ထပ် သုတေသနပြုလုပ်ရန် လိုအပ်ပါသည်။
HBOT ၏ ပိုးမွှားတိုက်ဖျက်နိုင်သော ဂုဏ်သတ္တိများ
HBOT မှ ဖန်တီးထားသော hyperoxidation ပတ်ဝန်းကျင်သည် ဘက်တီးရီးယားပိုးများကို တိုက်ဖျက်နိုင်သော ဂုဏ်သတ္တိများကို လှုံ့ဆော်ပေးသည့် ဇီဝကမ္မဗေဒနှင့် ဇီဝဓာတုဗေဒဆိုင်ရာ ပြောင်းလဲမှုများကို စတင်စေပြီး ရောဂါပိုးဝင်ခြင်းအတွက် ထိရောက်သော adjunct therapy တစ်ခု ဖြစ်စေသည်။ HBOT သည် တိုက်ရိုက် ဘက်တီးရီးယားပိုးများကို သေစေနိုင်သော လုပ်ဆောင်ချက်၊ ကိုယ်ခံအား တုံ့ပြန်မှုများ မြှင့်တင်ခြင်းနှင့် သီးခြား ပိုးသတ်ဆေးများနှင့် ပေါင်းစပ်အကျိုးသက်ရောက်မှုများကဲ့သို့သော ယန္တရားများမှတစ်ဆင့် aerobic bacteria နှင့် အဓိကအားဖြင့် anaerobic bacteria များအပေါ် သိသာထင်ရှားသော အကျိုးသက်ရောက်မှုများကို ပြသသည်။
၂.၁ HBOT ၏ တိုက်ရိုက် ဘက်တီးရီးယားပိုးသတ်ဆေး အာနိသင်များ
HBOT ၏ တိုက်ရိုက် ဘက်တီးရီးယား တိုက်ဖျက်နိုင်စွမ်းကို အဓိကအားဖြင့် ဆဲလ်ဇီဝဖြစ်စဉ်အတွင်း ပေါ်ပေါက်လာသော superoxide anions၊ hydrogen peroxide၊ hydroxyl radicals နှင့် hydroxyl ions များ ပါဝင်သော reactive oxygen species (ROS) များ ဖြစ်ပေါ်ခြင်းကြောင့် ဖြစ်သည်။
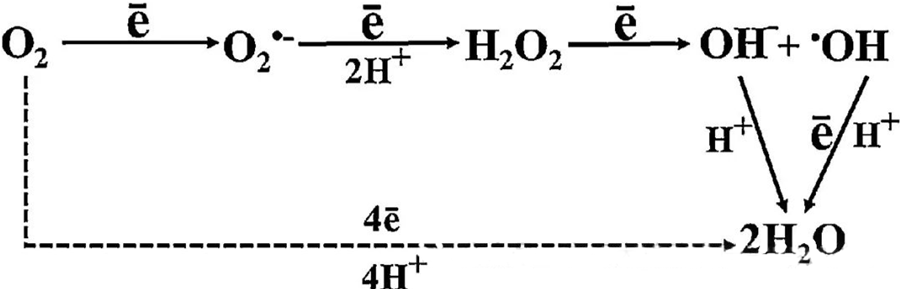
ဆဲလ်များအတွင်း ROS မည်သို့ဖွဲ့စည်းသည်ကို နားလည်ရန်အတွက် O₂ နှင့် ဆဲလ်အစိတ်အပိုင်းများအကြား အပြန်အလှန် ဆက်သွယ်မှုသည် မရှိမဖြစ် လိုအပ်ပါသည်။ အောက်ဆီဒေးရှင်းဖိစီးမှုဟု ရည်ညွှန်းသော အခြေအနေအချို့တွင်၊ ROS ဖွဲ့စည်းမှုနှင့် ၎င်း၏ ပြိုကွဲမှုကြား ဟန်ချက်ညီမှုသည် ပျက်ယွင်းသွားပြီး ဆဲလ်များတွင် ROS အဆင့် မြင့်မားလာစေသည်။ စူပါအောက်ဆိုဒ် (O₂⁻) ထုတ်လုပ်မှုကို စူပါအောက်ဆိုဒ် ဒစ်မူတေ့စ်က ဓါတ်ကူပေးပြီး နောက်ပိုင်းတွင် O₂⁻ ကို ဟိုက်ဒရိုဂျင်ပါအောက်ဆိုဒ် (H₂O₂) အဖြစ်သို့ ပြောင်းလဲပေးသည်။ ဤပြောင်းလဲခြင်းကို Fenton ဓာတ်ပြုမှုဖြင့် ပိုမိုအားကောင်းစေပြီး၊ ၎င်းတွင် Fe²⁺ ကို အောက်ဆီဒေးရှင်းလုပ်ပြီး ဟိုက်ဒရောက်ဆီလ် ရယ်ဒီကယ် (·OH) နှင့် Fe³⁺ တို့ကို ထုတ်လုပ်ပေးပြီး ROS ဖွဲ့စည်းမှုနှင့် ဆဲလ်ပျက်စီးမှုတို့၏ အန္တရာယ်ရှိသော ရီဒေါ့စ် အစီအစဉ်တစ်ခုကို စတင်စေသည်။
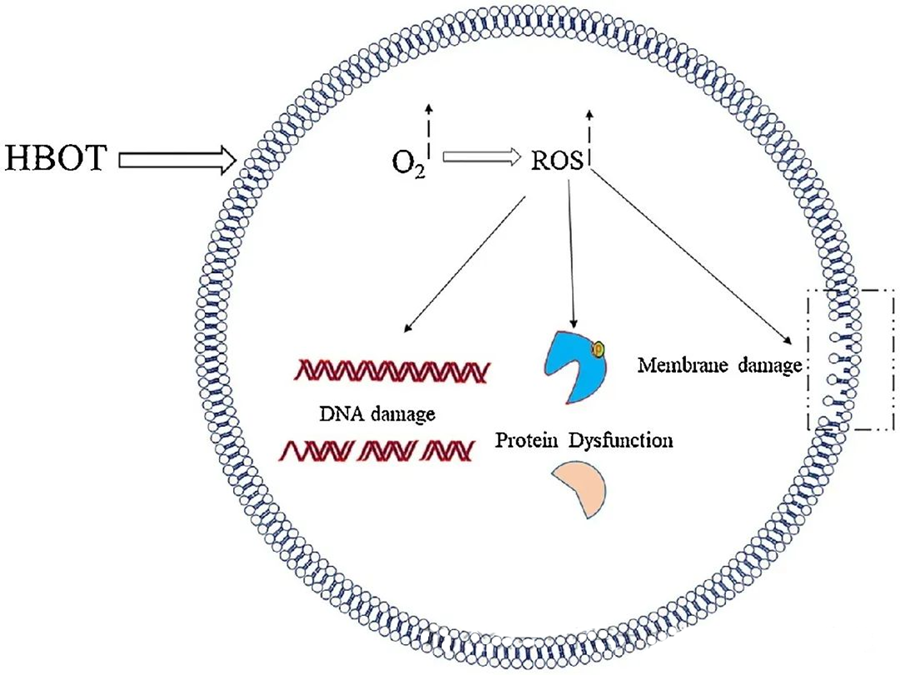
ROS ၏ အဆိပ်အတောက်ဖြစ်စေသော အာနိသင်များသည် DNA၊ RNA၊ ပရိုတင်းများနှင့် lipid ကဲ့သို့သော အရေးကြီးဆဲလ်အစိတ်အပိုင်းများကို ပစ်မှတ်ထားသည်။ မှတ်သားစရာကောင်းသည်မှာ DNA သည် deoxyribose ဖွဲ့စည်းပုံများကို အနှောင့်အယှက်ပေးပြီး အခြေခံဖွဲ့စည်းမှုများကို ပျက်စီးစေသောကြောင့် H₂O₂-mediated cytotoxicity ၏ အဓိကပစ်မှတ်တစ်ခုဖြစ်သည်။ ROS ကြောင့် ဖြစ်ပေါ်လာသော ရုပ်ပိုင်းဆိုင်ရာပျက်စီးမှုသည် DNA ၏ helix ဖွဲ့စည်းပုံအထိ ကျယ်ပြန့်ပြီး ROS ကြောင့် ဖြစ်ပေါ်လာသော lipid peroxidation ကြောင့် ဖြစ်ပေါ်လာနိုင်သည်။ ၎င်းသည် ဇီဝဗေဒဆိုင်ရာစနစ်များအတွင်း ROS အဆင့်မြင့်မားခြင်း၏ ဆိုးကျိုးများကို အလေးပေးဖော်ပြသည်။
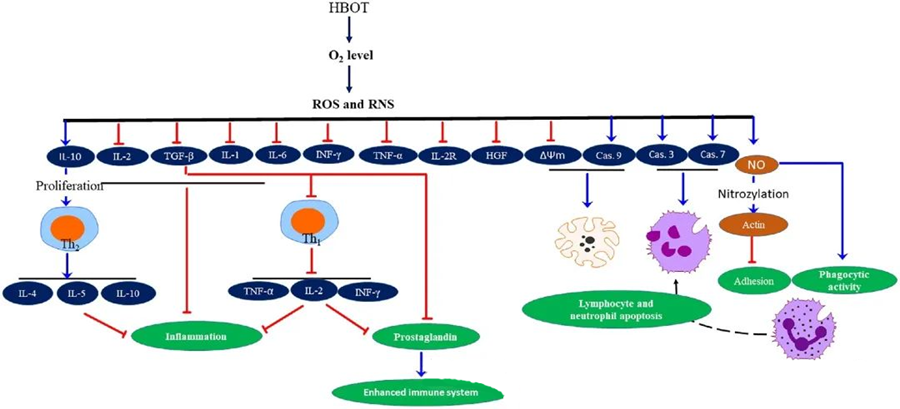
ROS ၏ အဏုဇီဝပိုးများကို တိုက်ဖျက်နိုင်သည့် လုပ်ဆောင်ချက်
HBOT ကြောင့်ဖြစ်ပေါ်လာသော ROS ထုတ်လုပ်မှုမှတစ်ဆင့်ပြသထားသည့်အတိုင်း ROS သည် အဏုဇီဝများကြီးထွားမှုကို ဟန့်တားရာတွင် အရေးကြီးသောအခန်းကဏ္ဍမှ ပါဝင်သည်။ ROS ၏ အဆိပ်သင့်အကျိုးသက်ရောက်မှုများသည် DNA၊ ပရိုတင်းများနှင့် lipid များကဲ့သို့သော ဆဲလ်အစိတ်အပိုင်းများကို တိုက်ရိုက်ပစ်မှတ်ထားသည်။ တက်ကြွသော အောက်ဆီဂျင်မျိုးစိတ်များ မြင့်မားစွာပါဝင်မှုသည် lipid များကို တိုက်ရိုက်ပျက်စီးစေပြီး lipid peroxidation ကို ဖြစ်ပေါ်စေသည်။ ဤလုပ်ငန်းစဉ်သည် ဆဲလ်အမြှေးပါးများ၏ တည်တံ့ခိုင်မြဲမှုကို ထိခိုက်စေပြီး ထို့ကြောင့် အမြှေးပါးနှင့်ဆက်စပ်သော receptors များနှင့် ပရိုတင်းများ၏ လုပ်ဆောင်နိုင်စွမ်းကို ထိခိုက်စေပါသည်။
ထို့အပြင်၊ ROS ၏ သိသာထင်ရှားသော မော်လီကျူးပစ်မှတ်များဖြစ်သည့် ပရိုတင်းများသည် cysteine၊ methionine၊ tyrosine၊ phenylalanine နှင့် tryptophan ကဲ့သို့သော အမိုင်နိုအက်ဆစ် အကြွင်းအကျန်အမျိုးမျိုးတွင် သီးခြားဓာတ်တိုးပြုပြင်မွမ်းမံမှုများကို ခံယူကြသည်။ ဥပမာအားဖြင့်၊ HBOT သည် elongation factor G နှင့် DnaK အပါအဝင် E. coli ရှိ ပရိုတင်းအများအပြားတွင် ဓာတ်တိုးပြောင်းလဲမှုများကို ဖြစ်ပေါ်စေပြီး ၎င်းတို့၏ ဆဲလ်လုပ်ဆောင်ချက်များကို ထိခိုက်စေကြောင်း ပြသထားသည်။
HBOT မှတစ်ဆင့် ကိုယ်ခံအား မြှင့်တင်ခြင်း
HBOT ၏ ရောင်ရမ်းမှုကို ဆန့်ကျင်သော ဂုဏ်သတ္တိများတစ်ရှူးပျက်စီးမှုကို သက်သာစေရန်နှင့် ရောဂါပိုးကူးစက်မှုတိုးတက်မှုကို နှိမ်နင်းရာတွင် အရေးကြီးကြောင်း သက်သေပြနေသည့် အထောက်အထားများကို မှတ်တမ်းတင်ထားပါသည်။ HBOT သည် cytokines နှင့် အခြားရောင်ရမ်းမှုထိန်းညှိပေးသည့်ပစ္စည်းများ၏ ဖော်ပြမှုကို သိသိသာသာ သက်ရောက်မှုရှိပြီး ကိုယ်ခံအားတုံ့ပြန်မှုကို လွှမ်းမိုးပါသည်။ စမ်းသပ်မှုစနစ်အမျိုးမျိုးသည် HBOT ပြီးနောက် မျိုးဗီဇဖော်ပြမှုနှင့် ပရိုတင်းထုတ်လုပ်မှုတွင် ကွဲပြားသောပြောင်းလဲမှုများကို တွေ့ရှိခဲ့ပြီး ၎င်းသည် growth factors နှင့် cytokines များကို မြှင့်တင်ခြင်း သို့မဟုတ် လျှော့ချခြင်းတို့ကို ဖြစ်စေပါသည်။
HBOT လုပ်ငန်းစဉ်အတွင်း O₂ အဆင့်များ မြင့်တက်လာခြင်းသည် ရောင်ရမ်းမှုကို ဖြစ်စေသော မီဒီယာများ ထုတ်လွှတ်မှုကို ဖိနှိပ်ခြင်းနှင့် လင့်ဖိုဆိုက်နှင့် နျူထရိုဖီးလ် အသေခံမှုကို အားပေးခြင်းကဲ့သို့သော ဆဲလ်တုံ့ပြန်မှုအမျိုးမျိုးကို လှုံ့ဆော်ပေးသည်။ စုပေါင်းအားဖြင့် ဤလုပ်ဆောင်ချက်များသည် ကိုယ်ခံအားစနစ်၏ ပိုးမွှားတိုက်ဖျက်သည့် ယန္တရားများကို မြှင့်တင်ပေးပြီး ရောဂါပိုးများကို ပျောက်ကင်းစေရန် လွယ်ကူချောမွေ့စေသည်။
ထို့အပြင်၊ HBOT အတွင်း O₂ အဆင့်များ မြင့်တက်လာခြင်းသည် interferon-gamma (IFN-γ), interleukin-1 (IL-1) နှင့် interleukin-6 (IL-6) အပါအဝင် ရောင်ရမ်းမှုကို ဖြစ်စေသော cytokines များ၏ ဖော်ပြမှုကို လျော့ကျစေနိုင်ကြောင်း လေ့လာမှုများက ဖော်ပြသည်။ ဤပြောင်းလဲမှုများတွင် CD4:CD8 T ဆဲလ်များ၏ အချိုးအစားကို လျှော့ချခြင်းနှင့် အခြားပျော်ဝင်နိုင်သော receptors များကို ပြုပြင်ပြောင်းလဲခြင်းလည်း ပါဝင်ပြီး၊ နောက်ဆုံးတွင် interleukin-10 (IL-10) အဆင့်များကို မြှင့်တင်ပေးခြင်း၊ ၎င်းသည် ရောင်ရမ်းမှုကို တန်ပြန်ရန်နှင့် အနာကျက်ခြင်းကို မြှင့်တင်ရန်အတွက် အရေးကြီးပါသည်။
HBOT ၏ အဏုဇီဝပိုးများ တိုက်ဖျက်နိုင်စွမ်းသည် ရှုပ်ထွေးသော ဇီဝဗေဒဆိုင်ရာ ယန္တရားများနှင့် ဆက်စပ်နေသည်။ စူပါအောက်ဆိုဒ်နှင့် မြင့်မားသောဖိအား နှစ်မျိုးလုံးသည် HBOT ကြောင့်ဖြစ်ပေါ်လာသော ဘက်တီးရီးယားပိုးမွှားများ တိုက်ဖျက်နိုင်စွမ်းနှင့် နျူထရိုဖီးလ်များ အသေခံပျက်စီးမှုကို မြှင့်တင်ပေးသည်ဟု သတင်းပို့ထားသည်။ HBOT ပြီးနောက် အောက်ဆီဂျင်အဆင့် သိသိသာသာ မြင့်တက်လာခြင်းသည် ကိုယ်ခံအားတုံ့ပြန်မှု၏ မရှိမဖြစ် အစိတ်အပိုင်းတစ်ခုဖြစ်သည့် နျူထရိုဖီးလ်များ၏ ဘက်တီးရီးယားပိုးများကို သေစေနိုင်သော စွမ်းရည်ကို မြှင့်တင်ပေးသည်။ ထို့အပြင်၊ HBOT သည် နျူထရိုဖီးလ်များပေါ်ရှိ β-integrins များသည် endothelial ဆဲလ်များပေါ်ရှိ intercellular adhesion molecules (ICAM) နှင့် အပြန်အလှန် ဆက်သွယ်မှုကြောင့် ဖြစ်ပေါ်လာသော နျူထရိုဖီးလ် ကပ်ငြိမှုကို ဖိနှိပ်ပေးသည်။ HBOT သည် နိုက်ထရစ်အောက်ဆိုဒ် (NO) ကြားဝင်လုပ်ငန်းစဉ်မှတစ်ဆင့် နျူထရိုဖီးလ် β-2 integrin (Mac-1, CD11b/CD18) ၏ လှုပ်ရှားမှုကို တားဆီးပေးပြီး ရောဂါပိုးကူးစက်ခံရသည့်နေရာသို့ နျူထရိုဖီးလ်များ ရွှေ့ပြောင်းခြင်းကို အထောက်အကူပြုသည်။
ရောဂါပိုးများကို ထိရောက်စွာ phagocytize လုပ်ရန်အတွက် neutrophils များအတွက် cytoskeleton ၏ တိကျသော ပြန်လည်စီစဉ်မှု လိုအပ်ပါသည်။ actin ၏ S-nitrosylation သည် actin polymerization ကို လှုံ့ဆော်ပေးသည်ဟု ပြသထားပြီး HBOT ကြိုတင်ကုသမှုပြီးနောက် neutrophils များ၏ phagocytic activity ကို အထောက်အကူပြုနိုင်သည်ဟု ယူဆရပါသည်။ ထို့အပြင်၊ HBOT သည် mitochondrial လမ်းကြောင်းများမှတစ်ဆင့် human T cell lines များတွင် apoptosis ကို မြှင့်တင်ပေးပြီး HBOT ပြီးနောက် lymphocyte သေဆုံးမှုကို အရှိန်မြှင့်ပေးသည်ဟု သတင်းပို့ထားပါသည်။ caspase-8 ကို မထိခိုက်စေဘဲ caspase-9 ကို ပိတ်ဆို့ခြင်းသည် HBOT ၏ immunomodulatory effect များကို ပြသခဲ့သည်။
HBOT နှင့် ပိုးမွှားတိုက်ဖျက်ဆေးများ၏ ပေါင်းစပ်အကျိုးသက်ရောက်မှုများ
ဆေးခန်းအသုံးချမှုများတွင် HBOT ကို ရောဂါပိုးများကို ထိရောက်စွာ တိုက်ဖျက်ရန်အတွက် ပဋိဇီဝဆေးများနှင့်အတူ မကြာခဏ အသုံးပြုလေ့ရှိသည်။ HBOT ကာလအတွင်း ရရှိလာသော အောက်ဆီဂျင်များလွန်းသော အခြေအနေသည် အချို့သော ပဋိဇီဝဆေးများ၏ ထိရောက်မှုကို လွှမ်းမိုးနိုင်သည်။ β-lactams၊ fluoroquinolones နှင့် aminoglycosides ကဲ့သို့သော သီးခြား ဘက်တီးရီးယားပိုးသတ်ဆေးများသည် မွေးရာပါ ယန္တရားများမှတစ်ဆင့် လုပ်ဆောင်ရုံသာမက ဘက်တီးရီးယားများ၏ aerobic ဇီဝဖြစ်စဉ်ပေါ်တွင်လည်း တစ်စိတ်တစ်ပိုင်း မူတည်ကြောင်း သုတေသနပြုချက်များက ဖော်ပြသည်။ ထို့ကြောင့် အောက်ဆီဂျင်ရှိနေခြင်းနှင့် ရောဂါပိုးများ၏ ဇီဝဖြစ်စဉ်ဆိုင်ရာ ဝိသေသလက္ခဏာများသည် ပဋိဇီဝဆေးများ၏ ကုထုံးဆိုင်ရာ အကျိုးသက်ရောက်မှုများကို အကဲဖြတ်ရာတွင် အဓိကကျသည်။
အောက်ဆီဂျင်အဆင့်နိမ့်ခြင်းသည် Pseudomonas aeruginosa ၏ piperacillin/tazobactam ကို ခံနိုင်ရည်ရှိစေကြောင်းနှင့် အောက်ဆီဂျင်နိမ့်သောပတ်ဝန်းကျင်သည် Enterobacter cloacae ၏ azithromycin ကို ခံနိုင်ရည်ရှိစေကြောင်း သိသာထင်ရှားသောအထောက်အထားများက ပြသထားသည်။ ဆန့်ကျင်ဘက်အားဖြင့် အောက်ဆီဂျင်နည်းပါးသောအခြေအနေအချို့သည် တက်ထရာဆိုက်ကလင်းပဋိဇီဝဆေးများအပေါ် ဘက်တီးရီးယားများ၏ အာရုံခံနိုင်စွမ်းကို တိုးမြင့်စေနိုင်သည်။ HBOT သည် aerobic metabolism ကိုလှုံ့ဆော်ပေးပြီး အောက်ဆီဂျင်နည်းပါးသောကူးစက်ခံထားရသောတစ်ရှူးများကို ပြန်လည်အောက်ဆီဂျင်ဖြည့်တင်းပေးခြင်းဖြင့် အသုံးဝင်သော adjunctive therapeutic method အဖြစ်ဆောင်ရွက်ပြီး နောက်ပိုင်းတွင် ရောဂါပိုးများ၏ ပဋိဇီဝဆေးများအပေါ် အာရုံခံနိုင်စွမ်းကို တိုးမြင့်စေပါသည်။
ကြိုတင်လေ့လာမှုများတွင်၊ tobramycin (တစ်နေ့လျှင် 20 mg/kg) နှင့်အတူ တစ်နေ့လျှင် နှစ်ကြိမ် 280 kPa တွင် ၈ နာရီကြာ ထိုးပေးသည့် HBOT ကို ပေါင်းစပ်အသုံးပြုခြင်းသည် Staphylococcus aureus ကူးစက်ရောဂါ endocarditis တွင် ဘက်တီးရီးယားပမာဏကို သိသိသာသာ လျော့ကျစေပါသည်။ ၎င်းသည် HBOT ၏ အရန်ကုသမှုအလားအလာကို ပြသနေပါသည်။ နောက်ထပ် စုံစမ်းစစ်ဆေးမှုများအရ 37°C နှင့် 3 ATA ဖိအားအောက်တွင် 5 နာရီကြာ HBOT သည် macrophage ကူးစက်ခံရသော Pseudomonas aeruginosa ကို imipenem ၏ အာနိသင်ကို သိသိသာသာ မြှင့်တင်ပေးကြောင်း ဖော်ပြသည်။ ထို့အပြင်၊ cephazolin နှင့် HBOT ကို ပေါင်းစပ်အသုံးပြုခြင်းသည် တိရစ္ဆာန်မော်ဒယ်များတွင် cephazolin တစ်ခုတည်းနှင့် နှိုင်းယှဉ်ပါက Staphylococcus aureus osteomyelitis ကို ကုသရာတွင် ပိုမိုထိရောက်ကြောင်း တွေ့ရှိခဲ့သည်။
HBOT သည် ciprofloxacin ၏ Pseudomonas aeruginosa biofilms များအပေါ် ဘက်တီးရီးယားပိုးများကို သေစေနိုင်သော အာနိသင်ကို သိသိသာသာ မြှင့်တင်ပေးပြီး အထူးသဖြင့် မိနစ် ၉၀ ထိတွေ့ပြီးနောက်တွင် ဖြစ်သည်။ ဤအာနိသင် တိုးလာခြင်းသည် endogenous reactive oxygen species (ROS) ဖွဲ့စည်းမှုကြောင့်ဖြစ်ပြီး peroxidase-defective mutants များတွင် ပိုမိုမြင့်မားသော sensitivity ကို ပြသသည်။
methicillin-resistant Staphylococcus aureus (MRSA) ကြောင့်ဖြစ်သော အဆုတ်ရောင်ရောဂါပုံစံများတွင် vancomycin၊ teicoplanin နှင့် linezolid တို့၏ HBOT နှင့် ပူးပေါင်းအာနိသင်သည် MRSA ကို သိသိသာသာ ထိရောက်မှုရှိကြောင်း ပြသခဲ့သည်။ ဆီးချိုခြေထောက်ပိုးဝင်ခြင်း (DFIs) နှင့် ခွဲစိတ်မှုနေရာပိုးဝင်ခြင်း (SSIs) ကဲ့သို့သော ပြင်းထန်သော anaerobic နှင့် polymicrobial ပိုးဝင်ခြင်းများကို ကုသရာတွင် ကျယ်ကျယ်ပြန့်ပြန့်အသုံးပြုသည့် ပဋိဇီဝဆေး Metronidazole သည် anaerobic အခြေအနေများတွင် ပိုမိုမြင့်မားသော အဏုဇီဝပိုးမွှားများကို တိုက်ဖျက်နိုင်သည့် အာနိသင်ကို ပြသခဲ့သည်။ in vivo နှင့် in vitro နှစ်မျိုးလုံးတွင် metronidazole နှင့် HBOT ပေါင်းစပ်အသုံးပြုခြင်း၏ synergistic antibacterial အာနိသင်များကို လေ့လာရန် အနာဂတ်လေ့လာမှုများ လိုအပ်ပါသည်။
ခုခံနိုင်စွမ်းရှိသော ဘက်တီးရီးယားများအပေါ် HBOT ၏ အဏုဇီဝပိုးများကို တိုက်ဖျက်နိုင်သည့် ထိရောက်မှု
ခံနိုင်ရည်ရှိသော မျိုးကွဲများ တိုးတက်ပြောင်းလဲလာခြင်းနှင့် ပျံ့နှံ့လာခြင်းနှင့်အတူ ရိုးရာပဋိဇီဝဆေးများသည် အချိန်ကြာလာသည်နှင့်အမျှ ၎င်းတို့၏ အာနိသင် ဆုံးရှုံးသွားလေ့ရှိသည်။ ထို့အပြင်၊ HBOT သည် များစွာသောဆေးဝါးခံနိုင်ရည်ရှိသော ရောဂါပိုးများကြောင့် ဖြစ်ပွားသော ရောဂါပိုးများကို ကုသခြင်းနှင့် ကာကွယ်ခြင်းတွင် မရှိမဖြစ်လိုအပ်ကြောင်း သက်သေပြနိုင်ပြီး ပဋိဇီဝဆေးကုသမှုများ မအောင်မြင်သည့်အခါ အရေးကြီးသော ဗျူဟာတစ်ခုအဖြစ် ဆောင်ရွက်ပေးသည်။ လေ့လာမှုများစွာတွင် ဆေးခန်းဆိုင်ရာ ခံနိုင်ရည်ရှိသော ဘက်တီးရီးယားများအပေါ် HBOT ၏ သိသာထင်ရှားသော ဘက်တီးရီးယားများကို သေစေနိုင်သော အာနိသင်များကို ဖော်ပြထားပါသည်။ ဥပမာအားဖြင့်၊ 2 ATM တွင် မိနစ် 90 ကြာ HBOT အစည်းအဝေးသည် MRSA ကြီးထွားမှုကို သိသိသာသာ လျော့ကျစေခဲ့သည်။ ထို့အပြင်၊ အချိုးပုံစံများတွင် HBOT သည် MRSA ကူးစက်မှုများကို ဆန့်ကျင်သော ပဋိဇီဝဆေးအမျိုးမျိုး၏ ဘက်တီးရီးယားပိုးသတ်ဆေးအာနိသင်ကို မြှင့်တင်ပေးခဲ့သည်။ OXA-48 ထုတ်လုပ်သော Klebsiella pneumoniae ကြောင့် ဖြစ်ပွားသော osteomyelitis ကို ကုသရာတွင် HBOT သည် မည်သည့် နောက်ဆက်တွဲ ပဋိဇီဝဆေးမျှ မလိုအပ်ဘဲ ထိရောက်မှုရှိကြောင်း အစီရင်ခံစာများက အတည်ပြုခဲ့သည်။
အကျဉ်းချုပ်အားဖြင့်၊ hyperbaric oxygen ကုထုံးသည် ရောဂါပိုးများ ထိန်းချုပ်ရေးအတွက် မျက်နှာစုံမှ ချဉ်းကပ်မှုတစ်ခုဖြစ်ပြီး ကိုယ်ခံအားတုံ့ပြန်မှုကို မြှင့်တင်ပေးသည့်အပြင် ရှိပြီးသား ပိုးသတ်ဆေးများ၏ ထိရောက်မှုကိုလည်း မြှင့်တင်ပေးပါသည်။ ပြည့်စုံသော သုတေသနနှင့် ဖွံ့ဖြိုးတိုးတက်မှုဖြင့် ပဋိဇီဝဆေးယဉ်ပါးမှု၏ အကျိုးသက်ရောက်မှုများကို လျော့ပါးစေနိုင်သည့် အလားအလာရှိပြီး ဘက်တီးရီးယားကူးစက်မှုများကို တိုက်ဖျက်ရာတွင် မျှော်လင့်ချက်ပေးပါသည်။
ပို့စ်တင်ချိန်: ၂၀၂၅ ခုနှစ်၊ ဖေဖော်ဝါရီလ ၂၈ ရက်

